Để hiểu được Amoniac là gì? tác dụng được với những chất nào? Các cách viết phương trình điều chế Amoniac ra N2, Cân bằng phương trình hóa học 2NH3 → 3H2 + N2. Mời các bạn đọc và các em học sinh cùng nhau đi tìm hiểu cách điều chế từ Amoniac ra N2 tác dụng với những chất nào nhé.
Chú ý :
Amonia là chất khí không màu, có mùi hắc đặc trưng. Nó nhẹ hơn không khí, mật độ của nó gấp 0,589 lần không khí. Nó dễ dàng hóa lỏng do có liên kết hydro mạnh giữa các phân tử; chất lỏng sôi ở −33,3 °C (−27,94 °F), và đóng băng thành tinh thể trắng [9] ở −77,7 °C (−107,86 °F).
Amonia có thể được khử mùi thuận tiện bằng cách cho nó phản ứng với natri bicacbonat hoặc axit axetic. Cả hai phản ứng này đều tạo thành muối amoni không mùi.
Phương trình hóa học: NH3 ra N2
2NH3 → 3H2 + N2
Trong đó :
NH3 là Dung dịch amoniac
H2 là khí hidro
N2 là khí nitơ
– Điều kiện phản ứng: Nhiệt độ: 500°C Xúc tác: Fe, P
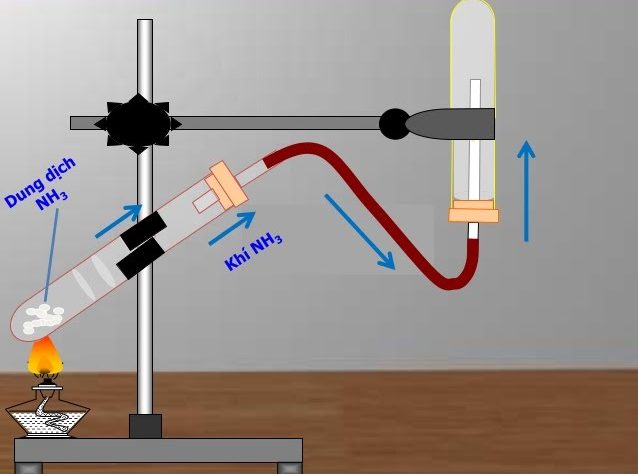
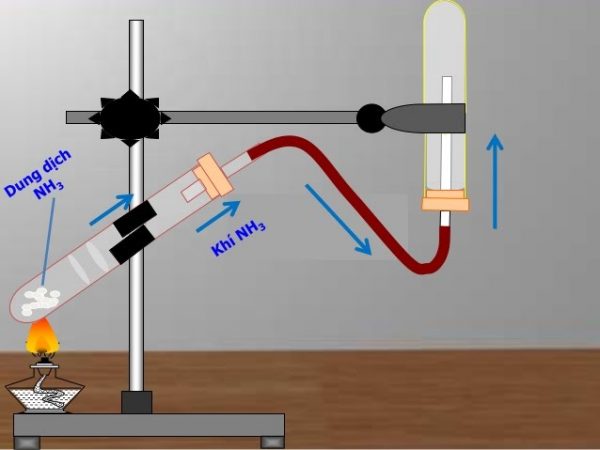
Thí nghiệm :
nhiệt phân dung dịch amoniac có khí thoát ra ngoài.
Điều chế nitơ từ amoniac :
Có nhiều phương trình điều chế nitơ từ amoniac. Dưới đây là một số phương trình:
2NH3 + 3PbO → 3H2O + N2 + 3Pb
3Cl2 + 2NH3 → 6HCl + N2
4NH3 + 3O2 → 6H2O + 2N2
2NH3 + 2CrO3 → 3H2O + N2 + Cr2O3
Cách điều chế Nito trong phòng thí nghiệm
Trong phòng thí nghiệm, N2 được điều chế bằng cách đun nóng dung dịch nước của amoni clorua và natri nitrit.
NH4Cl + Na2NO → NaCl + 2H2O + N2
Một lượng nhỏ oxit nitric và axit nitric cũng được tạo thành trong phản ứng này. Do đó, khí N2 thu được được tinh chế bằng cách cho khí sinh ra đi qua dung dịch axit sunfuric trong nước có chứa kali dicromat.
Ngoài ra, còn một số cách Cách điều chế Nito trong phòng thí nghiệm như:
1. Điều chế khí nito Bằng cách oxy hóa amoniac
Khi amoniac bị oxi hóa bởi một oxit đồng nóng đỏ hoặc bằng clo, người ta thu được nitơ. Điều chế khí nito
2NH3 + 3CuO → N2 + 3H2O + 3Cu
8NH3 + 3Cl2 → N2 + 6NH4Cl
2. Phân hủy nhiệt của amoni dicromat
Khi các tinh thể amoni dicromat màu đỏ được đun nóng, một phản ứng dữ dội xảy ra kèm theo các tia sáng và sự phát triển của nitơ.
(NH4)2Cr2O7 → N2 + 4H2O + Cr2O3
3. Bằng cách phân hủy nhiệt của Natri Azide
Điều chế khí nito rất tinh khiết có thể thu được bằng cách đun nóng natri hoặc bari azit.
2NaN3 → 2Na + 3N2
Ba (N3)2 → Ba + 3N2
Xem thêm các phương trình phản ứng NH3 khác :